De genterapier som används idag är främst utvecklade för monogena sjukdomar som orsakas av mutationer i en enda gen, och för olika typer av blodcancer. De genterapier som utvecklas för att behandla cancer kallas CAR-T-cellterapier (eller bara CAR-T) och är både är en form av genterapi och immunterapi.
En ny terapeutisk gen
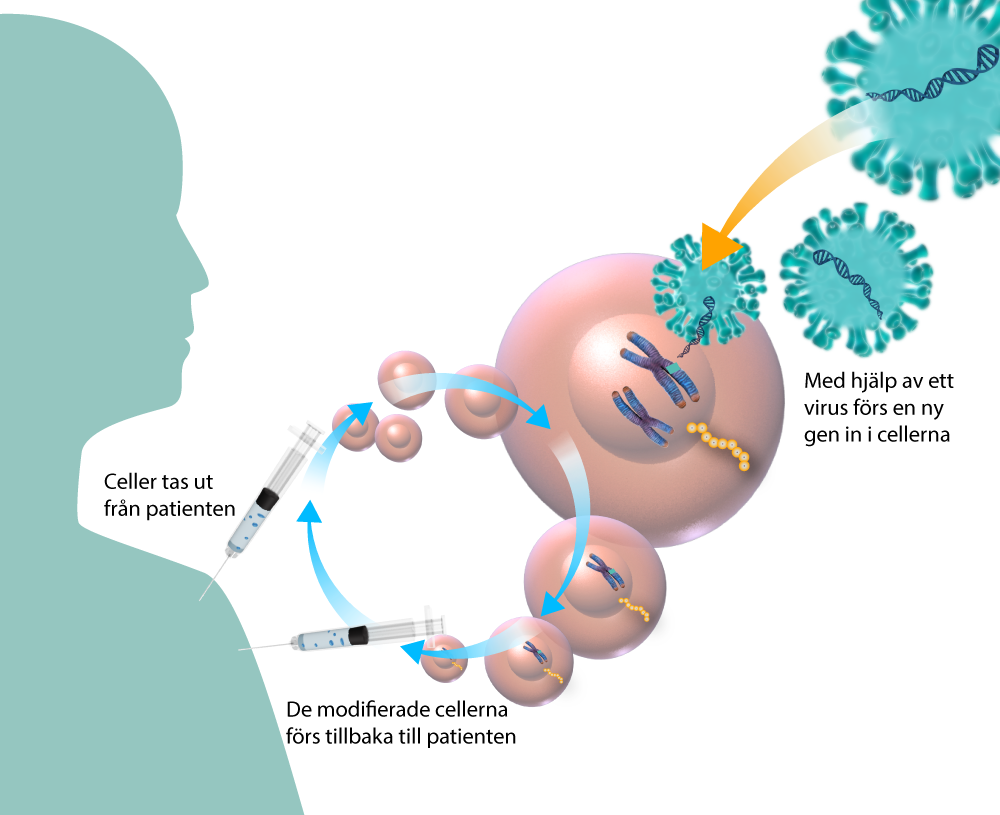
Vid den hittills vanligaste formen av genterapi förs en ny gen in i patientens celler. Den nya genens uppgift är att kompensera för en muterad gen som orsakar sjukdom. En gen kan till exempel ha muterat så att ett protein tillverkas felaktigt. Då kan den nya ”friska” genen kompensera för det och ge cellerna nya instruktioner om hur proteinet ska tillverkas.
Den här formen av genterapi kan liknas vid en transplantation där en ny gen förs in i kroppen istället för ett nytt organ. Effekten blir bestående eftersom allt DNA kopieras inför celldelning.
Den nya genen kan föras in i celler ex vivo, det vill säga ”utanför kroppen”. Det innebär att en grupp målceller som är inblandade i sjukdomen kan isoleras från patienten. Alla celler i hela kroppen får inte den nya genen. Efter att den terapeutiska genen förts in i cellerna försökas de upp och återförs till patienten som behandling. Beroende på vilken sjukdom som ska behandlas är målcellerna olika men oftast kan de utvinnas ur ett blod eller benmärgsprov.
Det finns också genterapier där celler modifieras med en ny gen in vivo, det vill säga när cellerna är kvar i patientens kropp. Det används när målcellerna inte kan isoleras, till exempel synceller i ögat.
Exempel på en genterapi som utförs ex vivo:
Strimvelis är en genterapi som utvecklats för en form av immunbristsjukdom som heter SCID (en förkortning av engelskans severe combined immune deficiency). Sjukdomen orsakas av en mutation i genen ADA och benämns därför ofta ADA-SCID. Mutationen leder till att det bildas för lite av ett enzym som behövs för att bygga upp ett normalt immunförsvar. Vid den genterapi som utvecklats för att behandla ADA-SCID isoleras stamceller från patienten och en ny ADA-gen förs in. När cellerna återförs gör den nya genen att enzymet börjar tillverkas och patienterna bygger upp ett normalt immunförsvar. Strimvelis är godkänd i Europa men ges endast på ett sjukhus i Italien.
Exempel på en genterapi som utförs in vivo:
Luxturna är en behandling för retinal dystrofi som är en form av ärftlig blindhet. Sjukdomen beror på en mutation i genen PRE65 som leder till en brist på ett enzym som krävs för att fotoreceptorcellerna (tapparna och stavarna) ska fungera. Genterapin ges som en injektion i ögats näthinna (retina) där det levererar en ny RPE65-gen som översätts till ett funktionellt enzym. Effekten av genterapin har varit olika men de flesta får en förbättrad ledsyn efter behandlingen. Luxturna är godkänd inom EU och används i Sverige.
För en lista av genterapier som EU-kommissionen godkänt se sidan Godkända genterapier.
Avväpnade virus transporterar gener
Virus har en speciell livsstrategi som går ut på att kapa funktioner hos sin värdorganism. Själva har virus ingen proteintillverkning och behöver därför hjälp med att göra nya virus. Ett virus är mycket mindre än en cell och kan ta sig in i celler och hela vägen in i cellkärnan där värdorganismens DNA lagras. Vissa typer av virus kan foga in sina gener i värdens genom medan andra lämnar det löst bredvid. På så sätt kidnappas värdcellens funktioner. Virusets gener översätts till virusproteiner som sätts samman till nya virus.

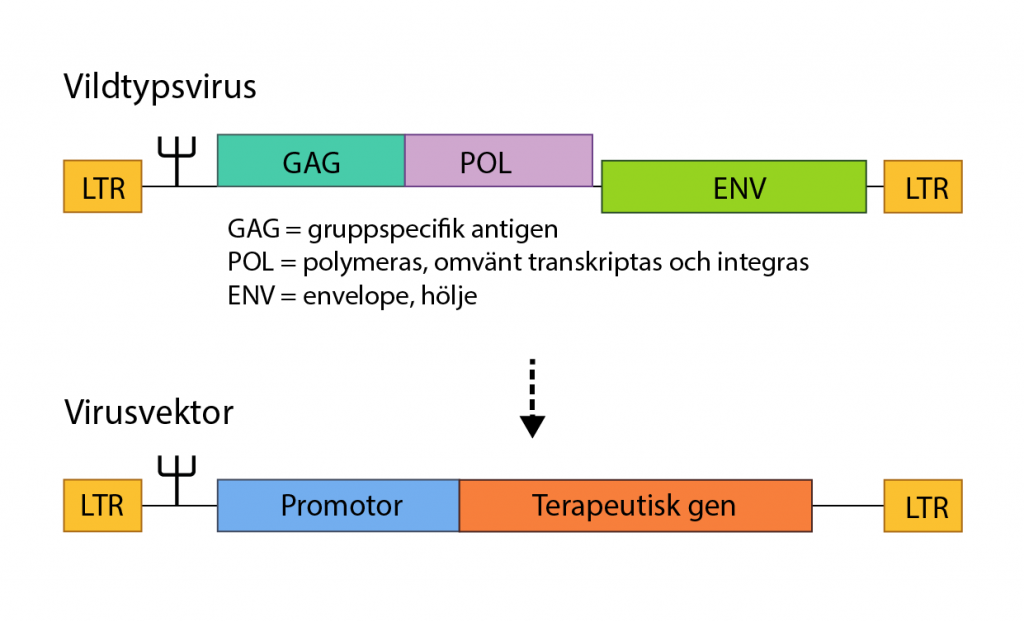
Under 1970-talet upptäckte forskare att det med genteknik går att omprogrammera virus och använda dem för att transportera andra gener än virusets egna. I genterapier har de gener som krävs för att viruset ska spridas tagits bort och ersatts med den terapeutiska genen. De vanligaste vektorerna är genetiskt modifierade retrovirus och adenovirus.
CAR-T är både en immunterapi och en genterapi
Till genterapier räknas också en typ av cancerbehandlingar som heter CAR-T-cellterapier, eller bara CAR-T. De är också som en form av immunterapi eftersom patientens eget immunförsvar riktas mot cancerceller.
Vid en behandling med CAR-T förs en ny gen in i en typ av immunceller som heter T-celler. Den nya genen kodar för en chimär antigen receptor och som förkortas CAR. Med CAR blir T-cellerna bättre på att upptäcka cancerceller via ett specifikt protein som finns på cancercellers utsida.
I de godkända CAR-T behandlingarna isoleras T-celler från patienten, och genen för CAR förs in i cellerna med hjälp av en virusvektor. Sedan förökas cellerna upp och återförs som behandling.
Bild från Depositphotos.
Information om hur CAR-T fungerar finns på sidan CAR-T (och CAR-NK).
Information om vilka CAR-T som är godkända inom EU finns på sidan Godkända genterapier.
En CRISPR-baserad genterapi är godkänd
Många genterapier som baseras på CRISPR/Cas och vidareutvecklingar av den tekniken är under utveckling. En har hittills godkänts av EU-kommissionen. Strategin bakom en CRISPR-baserad behandling är inte att föra in en ny terapeutisk gen, utan att ändra i patientens egna DNA. Det kallas för genomredigering, eller genredigering. I de första studierna användes CRISPR/Cas9 för att stänga av gener som orsakar sjukdom, men det är även möjligt att korrigera en specifik mutation i en gen.
Ett exempel på en genterapi där CRISPR/Cas9 används
Casgevy är utvecklad för behandling av hemoglobinsjukdomarna sicklecellanemi och beta thalassemi. Båda sjukdomarna orsakas av mutationer i HBB som är en av de gener som kodar för hemoglobin. Hos patienter med sjukdomarna tillverkas inte funktionellt hemoglobin vilket gör att blodet inte på ett effektivt sätt kan transportera syre i kroppen. Patienter får symtom som till exempel blodproppar, blodbrist och svår smärta till följd av syrebrist i vävnader och organ.
Det finns en annan form av hemoglobin som kan kompensera för bristen av funktionellt hemoglobin. Det bildas under fosterstadiet och kallas fetalt hemoglobin. En transkriptionsfaktor som heter BCL11A som stänger av tillverkningen av fetalt hemoglobin efter födseln. Strategin bakom genterapin är att med CRISPR/Cas9 stänga av den gen som kodar för transkriptionsfaktorn i blodbildande stamceller. Då återupptas tillverkningen av fetalt hemoglobin.
Behandlingen har gett mycket positiv effekt och nästan alla patienter som mottagit den är inte längre i behov av annan behandling. De är också i stort sett symtomfria. Det var med den här genterapin som forskare för första gången visade att en CRISPR/Cas9-baserad genterapi fungerade och det var också den första som godkändes för användning.
Genterapi utförs inte i könsceller och modifieringen blir därför inte ärftlig
När man talar om genterapi är det viktigt att skilja på vilka slags celler som används, eftersom det avgör om den genetiska modifieringen blir ärftlig eller inte. Den form av genterapi som används utförs i somatiska celler och inte könsceller. Den är därför inte ärftlig utan påverkar bara patienten som mottar behandlingen. Det kallas för somatisk genterapi (somatiska celler = kroppsceller).
När könsceller (ägg, spermier) eller befruktade ägg modifieras kan modifieringen nedärvas till nästa generation. Det är inte lagligt att utföra den typen av förändringar på människor, bland annat enligt lagen om genetisk integritet.
Det är dock tillåtet för forskare med särskilda etiska tillstånd att forska på ägg som befruktats in vitro upp till 14 dagar efter befruktningen. Det är viktigt att påpeka att de modifierade äggen absolut inte får föras in i en kvinnas livmoder där de kan leda till en graviditet.
Oligonukleotider som tystar gener
En annan form av behandlingar baseras på så kallade oligonukleotider. Oftast räknas inte dessa behandlingar som genterapier eftersom de inte resulterar i några förändringar på DNA-nivå.
Oligonukleotider är korta RNA-sekvenser som kan påverka uttrycket (aktiviteten) av gener. Det här kan till exempel användas för att ”tysta” en gen som orsakar sjukdom.
I ett första steg när en gen översätts till ett protein så bildas en kopia av genen i form av ett budbärar-RNA (mRNA). Det sker inne i cellkärnan där nästan allt vårt DNA ligger förvarat i kromosomer. De instruktioner som finns i genen transporteras ut ur cellkärnan med kopian (mRNA) till cellens proteinfabriker, ribosomerna.
Antisens och siRNA
En typ av oligonukleotid som används för att behandla vissa sjukdomar är ett så kallat antisens. Ett antisens-RNA kan konstrueras för att binda komplementärt till ett visst mRNA. När ett antisens binder till ”sitt” mRNA så inaktiveras det och tar sig aldrig till proteinfabriken.
En annan typ av oligonukleotid som används vid behandling av vissa sjukdomar är interfererande RNA (på eng. small interfering RNA, siRNA) som istället bryter ner ett specifikt mRNA innan det hinner översätts till ett protein. När ett mRNA inte översätts till ett protein så kan man säga har genen dämpats, eller helt stängts av.
Exempel på behandlingar med oligonukleotider
För en sjukdom som heter ärftlig transtyretinamyloidos som även kallas Skelleftesjukan, finns två tillgängliga läkemedel som bygger på oligonukleotider. Sjukdomen orsakas av en mutation som gör att proteinet transtyretin byggs upp felaktigt och klumpar ihop sig och lagras i olika vävnader. Inlagringen skadar bland annat nerver, hjärtat, ögonen och njurarna. På sikt leder sjukdomen till en progressiv funktionsnedsättning som kan vara livshotande.
I det ena läkemedlet används siRNA och i den andra ett antisens, men gemensamt för båda är att tillverkningen av transtyretin stängs av. Behandlingarna ges regelbundet med några veckors mellanrum.
En CRISPR/Cas9-baserad behandling för Skelleftesjukan är också under utveckling men är ännu inte godkänd. Mer information om behandlingen finns i artikeln CRISPR-baserad genterapi mot Skellftesjukan.
Uppdaterades 2026-03-13
